Waterstof en
Brandstofceltechnologie
Waterstof kan worden geproduceerd met behulp van duurzame energie, zoals zonne- of windenergie, wanneer electrolyzers worden gebruikt. Dit zijn in essentie “omgekeerde” brandstofcellen waarin waterstof wordt geproduceerd door water te splitsen in zuurstof en waterstof. Waterstof wordt gebruikt als energiedrager en biedt een realistische oplossing voor energieopslag op grote schaal, bijvoorbeeld voor het balanceren van het hernieuwbare energienetwerk.
Wanneer waterstof wordt verbrand komt er alleen warmte en water vrij, vandaar ook de Engelse naam hydrogen: “watervormer” in het oud-Grieks. In onze brandstofcelmodules wordt waterstof op een meer gecontroleerde manier omgezet in water, waarbij warmte en elektriciteit vrijkomt in plaats van vlammen. De elektrische energie kunnen we nuttig gebruiken, bijvoorbeeld om te rijden, varen, of vliegen.
PEM Brandstofcellen
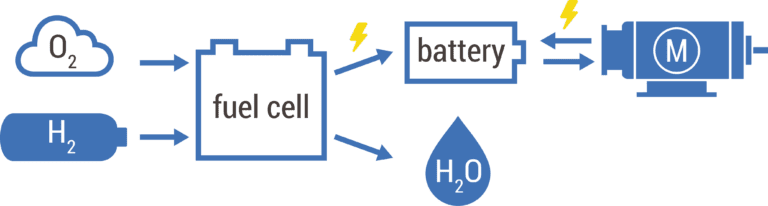
In onze systemen wordt waterstof gecombineerd met zuurstof uit de omgevingslucht om de chemische energie die is opgeslagen in deze moleculen om te zetten in elektrische energie en waterdamp. De elektrische energie die bij deze elektrochemische reactie vrijkomt, kan worden gebruikt om iedere toepassing van stroom te voorzien.
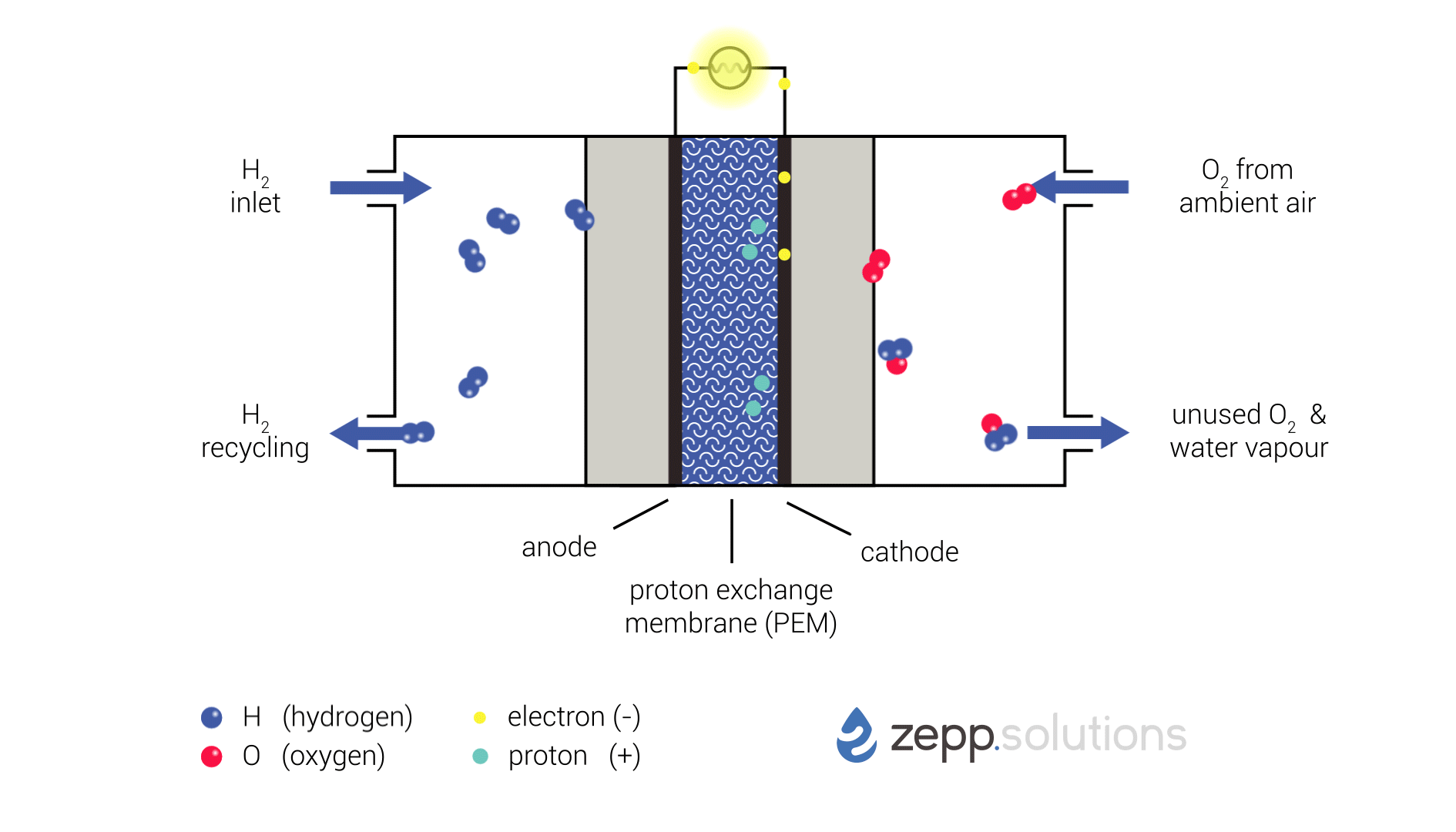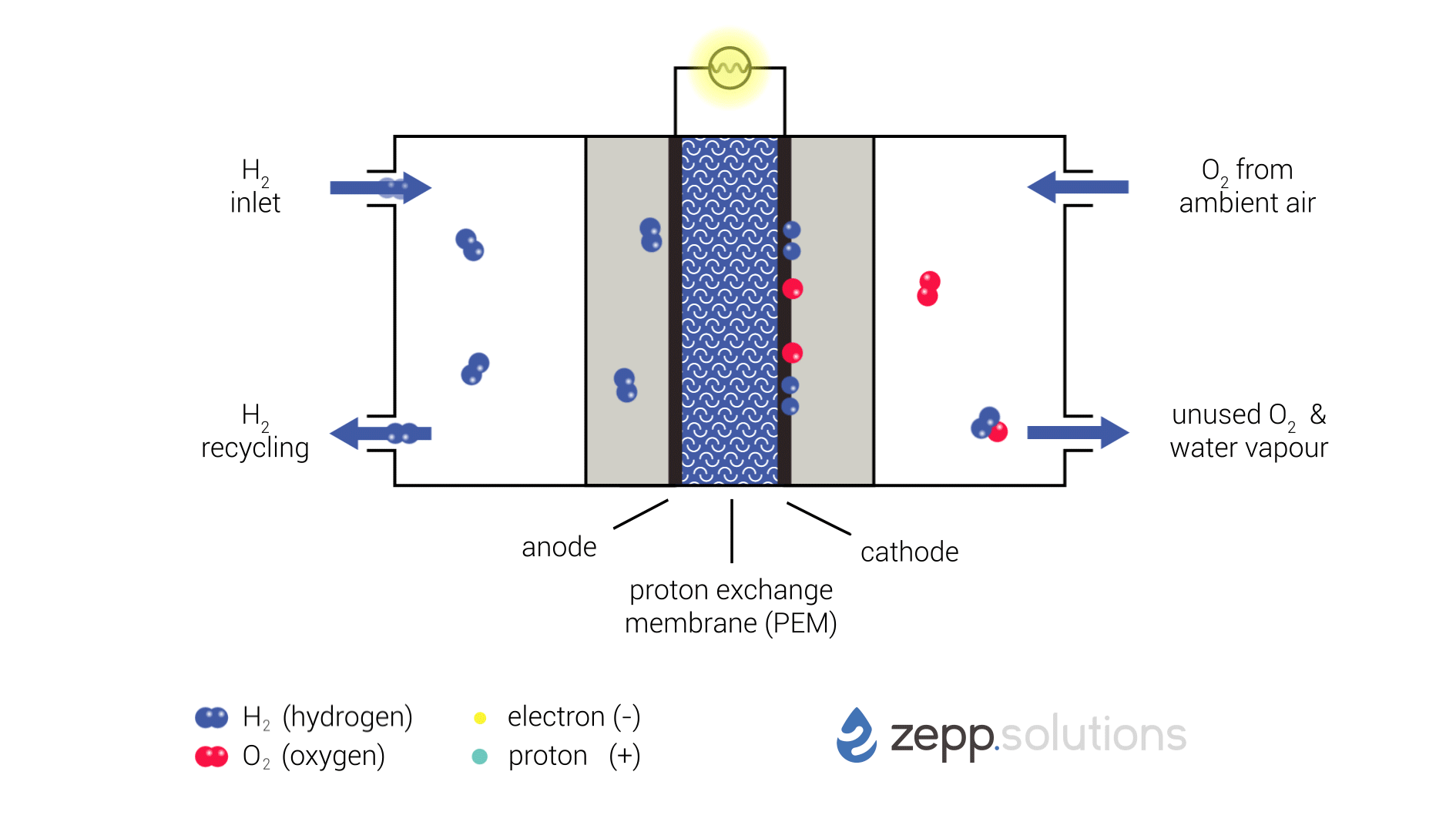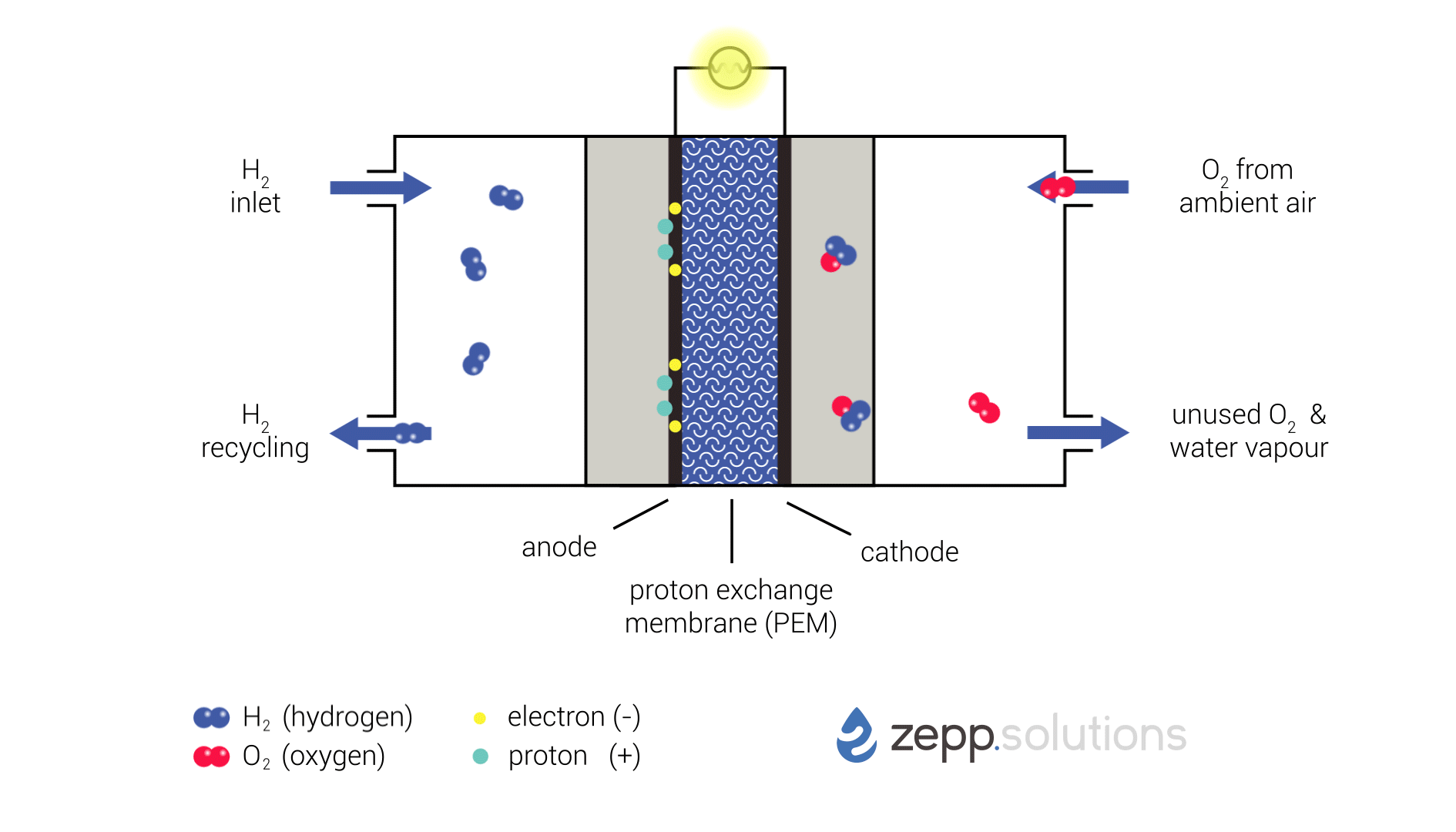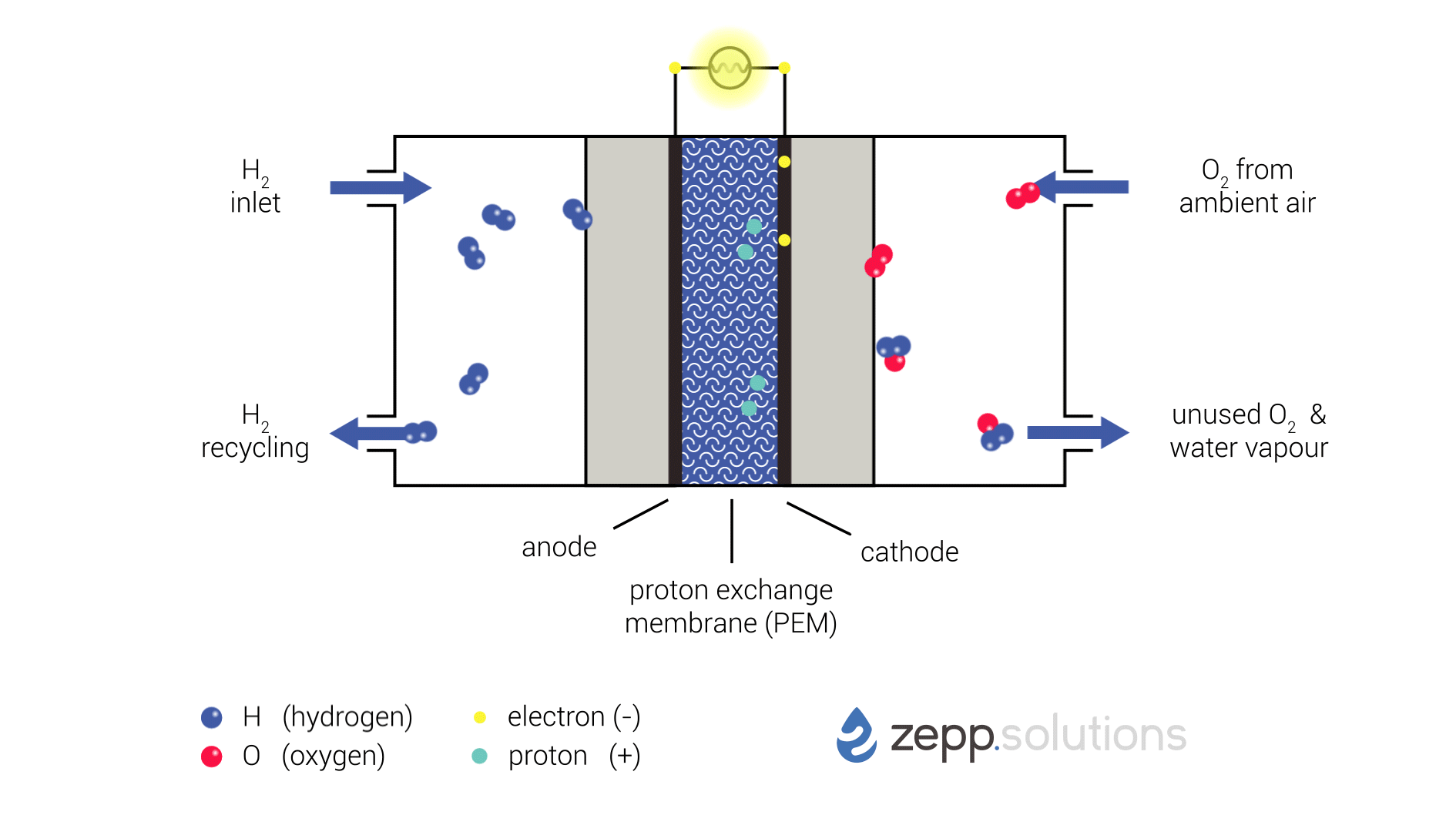
In onderstaande infographic wordt dit proces schematisch weergegeven. Waterstof komt de brandstofcel linksboven binnen en splitst zich aan de anodezijde van de cel met behulp van een katalysator in twee protonen en twee elektronen. Waterstof die niet reageert wordt gerecirculeerd en op een later tijdstip opnieuw in de cel geïntroduceerd. In de kern van de cell bevindt zich een “Proton Exchange Membrane” (PEM). Deze heeft als eigenschap dat het wel protonen kan doorlaten, maar elektrisch isolerend is. De protonen kunnen het membraan passeren naar de cathode zijde van de cell. De elektronen zijn gedwongen om via een extern circuit de andere zijde, de kathode, te bereiken. Daar worden de elektronen, protonen en zuurstofmoleculen door middel van een katalysator samengevoegd tot H2O, water.
Hydrogen fuel cell technology is especially attractive for applications that combine a demand for high continuous power output with long operational uptimes. Current alternative energy storage systems, such as battery technology, require long charging times and the costs of these systems scale linearly with the required energy content. Twice the amount of energy requires twice the number of batteries, costing twice as much. For hydrogen-electric systems, only the amount of hydrogen storage has to be doubled, the fuel cell remains the same. Additionally, these operations benefit strongly from the quick refueling capabilities hydrogen fuel cell systems offer.
Hybride brandstofceltechnologie
Om onze klanten een optimale emissievrije aandrijflijn te bieden, ontwikkelen we op maat gemaakte hybride brandstofcelsystemen. Hierbij wordt waterstof brandstofceltechnologie gecombineerd met een kleine batterij die optimaal is afgestemd op de applicatie. Onze kerncompetenties zijn de (economische) configuratie, integratie en operationele aansturing van deze klantspecifieke systemen.
Het resultaat is een uniek ontworpen hybride brandstofcelsysteem, waarin het beste van waterstof- en batterijtechnologie wordt gecombineerd. Korte tanktijden en lange autonome operaties met hoge energiebehoeften zijn nu mogelijk, terwijl een vermogenspiek zonder vertraging kan worden beantwoord. Dit systeem wordt geoptimaliseerd naar een minimale Total Cost of Ownership, maar met een hoogstaande kwaliteit.